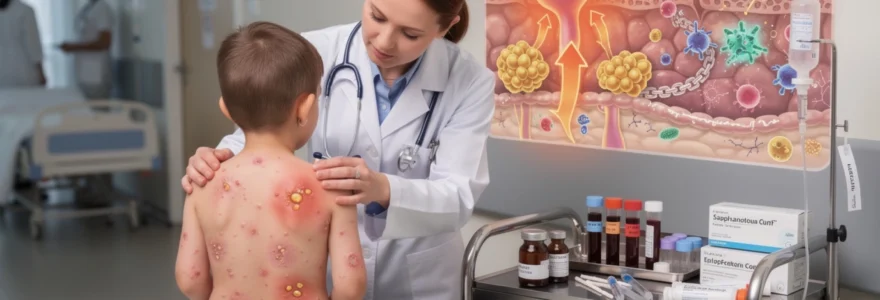
La varicelle, cette maladie infantile courante causée par le virus Varicella-Zoster (VZV), touche chaque année près de 700 000 enfants en France. Si elle est généralement bénigne, elle peut parfois se compliquer d’une surinfection bactérienne qui transforme cette affection virale en urgence médicale. Ces complications surviennent chez 2 à 4% des patients atteints de varicelle et représentent la principale cause d’hospitalisation liée à cette maladie. La reconnaissance précoce des signes de surinfection devient alors cruciale pour éviter des conséquences potentiellement graves, allant de l’impétigo simple à la fasciite nécrosante. Comprendre les mécanismes physiopathologiques, les signes cliniques d’alerte et les protocoles thérapeutiques appropriés permet aux professionnels de santé d’optimiser la prise en charge de ces complications infectieuses.
Physiopathologie de la surinfection bactérienne des lésions varicelleuses
Mécanismes d’invasion microbienne par staphylococcus aureus et streptococcus pyogenes
La surinfection bactérienne de la varicelle résulte d’une invasion opportuniste de la peau lésée par des pathogènes cutanés commensaux ou environnementaux. Staphylococcus aureus représente l’agent pathogène le plus fréquemment isolé, responsable de 60 à 70% des surinfections. Ce micro-organisme exploite sa capacité d’adhésion aux protéines de la matrice extracellulaire exposées dans les vésicules rompues. Streptococcus pyogenes, quant à lui, constitue le second agent pathogène en fréquence et présente un tropisme particulier pour les tissus mous, expliquant sa propension à causer des cellulites et des fasciites nécrosantes.
L’invasion bactérienne s’initie généralement au niveau des vésicules rompues spontanément ou par grattage. Les bactéries pénètrent dans les couches profondes de l’épiderme et du derme superficiel, où elles rencontrent un environnement favorable à leur multiplication. La température locale élevée, l’humidité des lésions et la richesse en débris cellulaires créent un milieu de culture optimal. Cette colonisation bactérienne peut rester localisée ou évoluer vers une diffusion systémique selon les facteurs de l’hôte et la virulence des micro-organismes impliqués.
Altération de la barrière cutanée par le virus Varicella-Zoster
Le virus VZV compromet l’intégrité de la barrière cutanée par plusieurs mécanismes complexes qui facilitent l’invasion bactérienne secondaire. L’infection virale provoque une cytopathogénicité directe des kératinocytes, entraînant leur destruction et la formation de vésicules intra-épidermiques caractéristiques. Cette lyse cellulaire expose les couches dermiques sous-jacentes, normalement protégées par l’épiderme intact.
La réplication virale active également une cascade inflammatoire locale qui perturbe l’homéostasie cutanée. Les médiateurs inflammatoires libérés, notamment les interleukines IL-1β et TNF-α, augmentent la perméabilité vasculaire et favorisent l’œdème tissulaire. Cette inflammation compromet également les mécanismes de défense antimicrobiens naturels de la peau, incluant la production de peptides antimicrobiens et l’activité des cellules dendritiques résidentes. La fonction barrière altérée persiste plusieurs jours
après l’apparition des premières vésicules, ce qui explique que la peau d’un enfant atteint de varicelle reste vulnérable aux bactéries bien au-delà du pic de l’éruption. Plus les lésions sont nombreuses et profondes, plus cette « porte d’entrée » pour les germes est large. Des facteurs mécaniques comme le grattage répété, le port de vêtements synthétiques irritants ou la macération liée au talc ou aux bains prolongés aggravent encore cette altération de la barrière cutanée et favorisent la surinfection bactérienne des boutons de varicelle.
Facteurs de virulence bactériens favorisant l’invasion tissulaire
La capacité des bactéries à transformer une varicelle simple en varicelle surinfectée repose en grande partie sur leurs facteurs de virulence. Staphylococcus aureus produit des toxines exfoliatives, des hémolysines et des leucocidines qui détruisent les kératinocytes, dissocient les couches de l’épiderme et facilitent la formation de bulles superficielles typiques de l’impétigo bulleux. Ses adhésines se lient aux fibronectines et à d’autres protéines de la matrice extracellulaire exposées par les vésicules de varicelle rompues, assurant un ancrage solide aux tissus cutanés.
Streptococcus pyogenes (streptocoque du groupe A) possède, quant à lui, une panoplie de facteurs de virulence qui expliquent la sévérité de certaines infections post-varicelle. La protéine M et la capsule de polysaccharides inhibent la phagocytose et permettent à la bactérie d’échapper aux défenses immunitaires innées. Les streptolysines, les DNases et les hyaluronidases dégradent activement les tissus, ouvrant la voie à une extension rapide de l’infection dans le derme profond, l’hypoderme et parfois jusqu’aux fascias musculaires. Dans les formes graves, les exotoxines pyrogènes agissent comme de véritables « superantigènes », déclenchant un choc toxique streptococcique.
On peut comparer ces facteurs de virulence à des outils spécialisés dont disposent les bactéries pour franchir, section par section, les couches protectrices de la peau. Plus l’arsenal est complet (toxinogénicité élevée, résistance à la phagocytose, capacité de diffusion tissulaire), plus le risque de cellulite ou de fasciite nécrosante post-varicelle est important. La co-infection staphylocoque–streptocoque n’est pas rare et associe alors les mécanismes pathogéniques des deux germes, rendant la prise en charge encore plus complexe.
Cascade inflammatoire et réponse immunitaire locale défaillante
La surinfection bactérienne des lésions de varicelle s’accompagne d’une cascade inflammatoire intense. Les produits bactériens (toxines, fragments de paroi, ADN bactérien) activent les récepteurs de l’immunité innée (récepteurs Toll-like, NOD-like) présents sur les kératinocytes, les macrophages tissulaires et les neutrophiles. Cette activation déclenche la libération de cytokines pro-inflammatoires (IL-1, IL-6, TNF-α) et de chimiokines recrutant massivement les polynucléaires neutrophiles vers le site infecté, ce qui explique la chaleur, la douleur et la rougeur périlésionnelle observées cliniquement.
Chez certains enfants, cette réponse immunitaire locale est insuffisante ou mal régulée. Un âge inférieur à un an, une immunodépression, une corticothérapie systémique ou l’usage d’anti-inflammatoires non stéroïdiens (AINS) dans le contexte de varicelle peuvent altérer la fonction des neutrophiles et des macrophages, ou en atténuer la mobilisation. À l’inverse, dans les formes fulminantes comme la fasciite nécrosante post-varicelle, la réponse inflammatoire devient systémique et disproportionnée, aboutissant à un syndrome de réponse inflammatoire systémique (SIRS) puis à un sepsis sévère. On peut ainsi voir la peau comme un « champ de bataille » : si les défenses locales sont débordées, les bactéries passent dans le sang et l’infection devient générale.
Diagnostic différentiel clinique des complications cutanées post-varicelleuses
Identification de l’impétigo bulleux secondaire à staphylococcus aureus
L’impétigo bulleux représente la forme la plus fréquente de surinfection bactérienne superficielle sur lésions de varicelle. Il survient souvent quelques jours après le début de l’éruption, lorsque les vésicules ont commencé à se rompre. Cliniquement, on observe l’apparition de bulles flasques, de taille variable, à contenu clair puis trouble, entourées d’un halo érythémateux. Ces bulles se développent sur ou à proximité des anciens boutons de varicelle, principalement sur le tronc, le visage et les plis.
Lorsque les bulles se rompent, elles laissent place à des érosions suintantes recouvertes de croûtes jaunâtres « mélicériques », typiques de l’impétigo staphylococcique. Contrairement à une varicelle simple, où toutes les lésions tendent à évoluer vers la croûte sèche en quelques jours, l’impétigo bulleux entraîne la persistance de zones humides, douloureuses ou prurigineuses, avec une extension centrifuge possible. La fièvre est modérée ou absente, mais l’atteinte peut devenir extensive chez le nourrisson ou l’enfant atopique. Vous vous demandez quand suspecter une varicelle surinfectée ? L’apparition de bulles nouvelles, de pus ou de croûtes épaisses et jaunâtres doit faire évoquer ce diagnostic.
Reconnaissance de la cellulite périvésiculaire streptococcique
La cellulite périvésiculaire streptococcique constitue une complication plus profonde des lésions de varicelle, impliquant le derme et l’hypoderme. Elle se manifeste par une zone étendue de rougeur vive, chaude, douloureuse au toucher, à bords souvent mal limités, entourant ou dépassant largement les anciennes vésicules. L’enfant présente généralement une fièvre plus élevée, une altération de l’état général, parfois des frissons et une sensation de malaise généralisé.
Contrairement à l’impétigo bulleux, la cellulite se caractérise par un œdème important des tissus sous-cutanés, pouvant provoquer une tension cutanée et une difficulté à mobiliser le segment atteint (par exemple, une jambe ou un bras). Les vésicules de varicelle situées dans la zone de cellulite prennent un aspect violacé ou nécrotique. Une progression rapide de la zone inflammatoire en quelques heures, associée à des douleurs disproportionnées à l’examen clinique, doit faire suspecter une atteinte plus profonde, telle qu’une fasciite nécrosante débutante, nécessitant une prise en charge urgente.
Critères diagnostiques de la fasciite nécrosante post-varicelle
La fasciite nécrosante post-varicelle, souvent due à Streptococcus pyogenes (parfois associé à Staphylococcus aureus), est une complication rare mais dramatique qui engage rapidement le pronostic vital. Elle survient typiquement chez l’enfant auparavant sain, quelques jours après le début de la varicelle, dans un contexte de surinfection cutanée. Les premiers signes peuvent mimer une cellulite classique, mais certaines caractéristiques doivent alerter : douleur très intense, mal contrôlée par les antalgiques habituels, extension rapide de l’érythème, aspect violacé ou grisâtre de la peau, apparition de bulles hémorragiques et signes généraux marqués (fièvre élevée, tachycardie, hypotonie).
Un signe majeur est la discordance entre l’aspect cutané initialement modéré et la douleur ressentie, souvent décrite comme insupportable par l’enfant. À un stade plus avancé, la peau devient froide, insensible par zones, avec crépitation possible à la palpation en cas de gaz dans les tissus. Ces éléments, associés à un syndrome inflammatoire biologique majeur et à un état de choc débutant, imposent une hospitalisation immédiate en milieu chirurgical et réanimatoire. On peut comparer la fasciite nécrosante à un « incendie souterrain » qui progresse sous la surface de la peau : tant que l’on ne l’a pas identifié, les tissus profonds continuent de se détruire rapidement.
Distinction entre eczéma herpéticum et surinfection bactérienne
L’eczéma herpéticum (ou pustulose varioliforme de Kaposi-Juliusberg) est une complication virale, le plus souvent liée au virus Herpes simplex, qui peut survenir sur une peau fragilisée par une dermatite atopique ou, plus rarement, après une varicelle récente. Il se manifeste par une éruption de vésicules et pustules ombiliquées, parfois hémorragiques, regroupées en nappes sur un fond érythémateux, s’accompagnant d’une fièvre élevée et d’une altération marquée de l’état général.
Différencier un eczéma herpéticum d’une surinfection bactérienne des lésions de varicelle repose sur plusieurs éléments : les lésions sont souvent plus monomorphes (toutes au même stade d’évolution), douloureuses plutôt que franchement purulentes, et peuvent s’étendre au visage, aux mains et aux zones eczémateuses préexistantes. La présence de petites vésicules ombiliquées, de ganglions cervicaux douloureux et un contexte d’herpès labial dans l’entourage orientent vers le diagnostic viral. En cas de doute, un prélèvement virologique et un avis dermatologique sont recommandés, car le traitement repose alors sur un antiviral systémique (aciclovir) et non sur une simple antibiothérapie.
Examens paracliniques et biomarqueurs diagnostiques spécialisés
Prélèvement bactériologique par écouvillonnage des lésions purulentes
Face à une varicelle surinfectée, le prélèvement bactériologique local par écouvillonnage est l’un des premiers examens à envisager. Il doit être réalisé sur une lésion fraîchement ouverte, après nettoyage soigneux à l’aide de sérum physiologique, en évitant les zones déjà traitées par des antiseptiques qui pourraient fausser les résultats. L’objectif est d’identifier avec précision l’agent responsable (staphylocoque, streptocoque ou autre germe) et de déterminer son profil de sensibilité aux antibiotiques.
En pratique courante, cet examen n’est pas systématique pour les surinfections cutanées modérées sans signe de gravité, traitées par une antibiothérapie probabiliste. Il devient en revanche indispensable dans les formes étendues, récidivantes, compliquées ou en cas d’échec d’un premier traitement. L’écouvillonnage permet également de dépister une infection par Staphylococcus aureus résistant à la méticilline (SARM), surtout en contexte communautaire ou hospitalier, et d’adapter rapidement la stratégie thérapeutique. Pour les parents, c’est souvent le seul examen « visible », simple et peu douloureux, mais son impact sur le choix de l’antibiotique est majeur.
Hémocultures et recherche de bactériémie associée
Les hémocultures sont indiquées dès que l’on suspecte une dissémination systémique de l’infection cutanée liée à la varicelle. Une fièvre élevée persistante, des frissons, une tachycardie, des marbrures cutanées, une baisse de la tension artérielle ou une altération brutale de l’état général doivent faire évoquer un sepsis secondaire à une varicelle surinfectée. Dans cette situation, il est crucial de prélever plusieurs paires d’hémocultures avant la première injection d’antibiotique intraveineux, afin d’augmenter la sensibilité de l’examen.
La mise en évidence de Streptococcus pyogenes ou de Staphylococcus aureus dans le sang confirme la bactériémie et permet d’adapter la durée et l’intensité de l’antibiothérapie. Elle oriente aussi le clinicien vers la recherche d’atteintes profondes associées, telles qu’une ostéomyélite, une pneumonie ou une endocardite, selon le contexte. Dans les formes sévères, la bactériémie est souvent l’arbre qui cache la forêt : elle témoigne d’une charge bactérienne importante et d’une rupture majeure des défenses de l’hôte.
Dosage de la procalcitonine et c-réactive protéine dans le sepsis cutané
Les biomarqueurs inflammatoires, en particulier la protéine C-réactive (CRP) et la procalcitonine (PCT), jouent un rôle d’appoint dans l’évaluation de la sévérité d’une varicelle surinfectée. La CRP augmente dans la plupart des infections bactériennes, mais aussi dans certaines infections virales ou situations inflammatoires non infectieuses. Un taux très élevé, associé à une leucocytose neutrophile, renforce l’hypothèse d’une cellulite profonde ou d’une fasciite nécrosante post-varicelle.
La procalcitonine, plus spécifique des infections bactériennes systémiques, peut aider à différencier une simple surinfection locale d’un sepsis en cours. Des valeurs élevées de PCT sont corrélées à la gravité de l’infection et au risque d’évolution défavorable. Toutefois, ces marqueurs ne remplacent ni l’examen clinique ni l’imagerie, ils les complètent. On peut les comparer à un « tableau de bord » biologique : ils signalent la gravité du terrain, mais ne disent pas à eux seuls où se situe précisément la lésion ni quel germe est en cause.
Imagerie par échographie doppler des tissus mous inflammatoires
L’échographie des tissus mous, associée au Doppler, est un outil de plus en plus utilisé dans l’exploration des complications cutanées de la varicelle. Elle permet de visualiser l’épaisseur du derme et de l’hypoderme, de détecter une collection liquidienne (abcès sous-cutané), un épanchement fascial ou un épaississement anormal des fascias. Dans le contexte d’une cellulite extensive ou d’une suspicion de fasciite nécrosante, l’échographie aide à orienter la décision de drainage chirurgical ou de simple traitement médical.
Le Doppler complète l’examen en évaluant la vascularisation des tissus inflammatoires. Une hypervascularisation diffuse évoque une cellulite, tandis qu’une hypovascularisation ou une absence de flux dans une zone suspecte peut traduire une nécrose tissulaire. L’échographie a l’avantage d’être non invasive, répétable et réalisable au lit du patient, y compris en pédiatrie. Dans certaines situations complexes, un scanner ou une IRM des tissus mous sera nécessaire pour cartographier précisément l’extension de la fasciite nécrosante et préparer l’intervention chirurgicale.
Protocoles thérapeutiques antibiotiques ciblés et résistances bactériennes
Le traitement d’une varicelle surinfectée repose sur une antibiothérapie adaptée à la gravité de l’atteinte cutanée et aux germes les plus probables. Dans les surinfections superficielles non compliquées (impétigo localisé, petites zones de surinfection autour de quelques boutons), un traitement par voie orale associant une pénicilline résistante aux pénicillinases ou une céphalosporine de première génération est souvent suffisant, en ciblant principalement Staphylococcus aureus sensible à la méticilline et les streptocoques. La durée habituelle du traitement se situe entre 5 et 7 jours, avec une réévaluation clinique précoce.
En cas de cellulite étendue, de fièvre élevée, d’atteinte du nourrisson ou d’immunodépression, une hospitalisation pour antibiothérapie intraveineuse s’impose. Des associations telles que une bêta-lactamine à large spectre (amoxicilline-acide clavulanique, céphalosporine de 2e ou 3e génération) avec éventuellement la clindamycine (utile pour inhiber la production de toxines streptococciques) sont recommandées. Dans les formes de sepsis sévère ou de choc toxique, la prise en charge suit les protocoles de réanimation (remplissage vasculaire, vasopresseurs, surveillance rapprochée) en complément de l’antibiothérapie.
La montée des résistances bactériennes, notamment des SARM communautaires, complique la prise en charge des varicelles surinfectées. Devant un contexte évocateur (antibiothérapies répétées, épidémie de SARM dans la région, échec d’un traitement de première ligne), il peut être nécessaire d’introduire d’emblée une molécule active sur les souches résistantes (par exemple, la vancomycine ou la teicoplanine en milieu hospitalier, ou le cotrimoxazole dans certains contextes communautaires, selon les recommandations locales). L’antibiogramme reste la boussole indispensable pour affiner ce choix.
Enfin, il convient de rappeler que les AINS (ibuprofène, kétoprofène) sont contre-indiqués dans le contexte de varicelle, en raison de leur association avec des formes cutanées graves (fasciite nécrosante, dermohypodermite nécrosante). La gestion de la douleur et de la fièvre doit reposer en priorité sur le paracétamol, en respectant les doses pédiatriques. L’éducation des parents à ce sujet fait partie intégrante de la prévention des surinfections graves.
Prévention primaire et mesures prophylactiques dermatologiques
La meilleure façon de réduire le risque de varicelle surinfectée reste la prévention primaire de l’infection virale elle-même. La vaccination contre la varicelle, recommandée en France chez les adolescents non immunisés et certains adultes à risque, permet de diminuer significativement l’incidence des formes graves et donc des surinfections cutanées. Dans les pays ayant adopté une vaccination universelle des nourrissons, on observe une baisse marquée des hospitalisations pour varicelle compliquée, y compris pour les cellulites et fasciites nécrosantes.
Sur le plan dermatologique, quelques mesures simples peuvent faire une réelle différence dans la prévention de la surinfection bactérienne des boutons de varicelle. Il est recommandé de maintenir une hygiène cutanée douce : douches courtes à l’eau tiède, avec un savon syndet ou un pain dermatologique non irritant, séchage par tamponnement sans frotter. Les bains prolongés et le talc sont à proscrire, car ils favorisent la macération et la prolifération bactérienne. Des antiseptiques aqueux (type chlorhexidine) peuvent être utilisés ponctuellement sur les lésions suintantes, en évitant les excès.
La prévention du grattage est un autre pilier essentiel. Couper les ongles courts, utiliser des moufles ou des chaussettes la nuit chez les plus petits, habiller l’enfant avec des vêtements amples en coton et maintenir une température ambiante fraîche limitent le prurit. Si les démangeaisons sont importantes, un antihistaminique sédatif peut être prescrit par le médecin. Expliquer aux parents que « chaque bouton arraché est une porte d’entrée potentielle pour les bactéries » aide souvent à renforcer l’observance de ces conseils.
Enfin, la vigilance des parents et des professionnels de santé sur l’apparition de rougeurs anormales, de pus, de bulles ou de douleur intense autour des lésions de varicelle est la clé d’un diagnostic précoce. En cas de doute, une consultation rapide permet de trancher entre simple irritation et début de varicelle surinfectée. Vous hésitez à consulter parce que votre enfant semble « seulement un peu plus rouge » que la veille ? Dans le contexte de varicelle, mieux vaut un avis médical de trop qu’un retard diagnostic devant une cellulite ou une fasciite débutante.
Complications systémiques graves et prise en charge hospitalière urgente
Dans un petit nombre de cas, la surinfection bactérienne des lésions de varicelle déborde le cadre cutané pour entraîner des complications systémiques graves. Outre la fasciite nécrosante et le choc toxique streptococcique déjà évoqués, on peut observer des pneumonies, des arthrites septiques, des ostéomyélites, voire des méningites bactériennes secondaires. Ces tableaux surviennent souvent chez l’enfant auparavant sain, ce qui les rend d’autant plus déroutants pour les familles. Les signes d’alerte incluent une fièvre persistante ou élevée, une altération rapide de l’état général, des douleurs articulaires ou osseuses localisées, une difficulté respiratoire ou des troubles de la conscience.
La prise en charge hospitalière de ces complications repose sur une approche multidisciplinaire associant pédiatres, infectiologues, chirurgiens et réanimateurs. L’initiation précoce d’une antibiothérapie intraveineuse à large spectre, ajustée secondairement selon les résultats microbiologiques, est impérative. En cas de fasciite nécrosante ou d’abcès profond, un débridement chirurgical urgent, parfois répété, est nécessaire pour contrôler le foyer infectieux. La réanimation hémodynamique (remplissage, vasopresseurs, oxygénothérapie, ventilation mécanique si besoin) vise à prévenir la défaillance multiviscérale.
Le pronostic dépend étroitement de la rapidité du diagnostic et de l’intervention. Chaque heure compte en cas de choc toxique ou de fasciite nécrosante post-varicelle. D’où l’importance d’informer clairement les parents des signes devant conduire à une consultation en urgence : douleur intense et inhabituelle, rougeur qui s’étend très vite, fièvre ne cédant pas au paracétamol, extrémités froides, respiration rapide, somnolence anormale. En parallèle, un soutien psychologique des familles est souvent nécessaire, tant l’écart est grand entre l’image d’une « simple maladie infantile » et la réalité d’une varicelle surinfectée nécessitant une hospitalisation lourde.
À l’échelle de la santé publique, ces formes graves rappellent que la varicelle, bien que fréquente et généralement bénigne, ne doit pas être banalisée. Une bonne information des parents, une prise en charge rigoureuse des boutons de varicelle et une vaccination adaptée constituent les trois leviers majeurs pour limiter le risque de surinfection bactérienne et de complications systémiques.